データの解釈について
中皮細胞面積の値と変動について
中皮細胞面積は50個を計測しその正規性から、平均±標準誤差(μ㎡)で示されている。よって、平均値は標準誤差の範囲で変動するということであり、最高値と最低値の両方を考慮する必要がある。我々はできるだけハイリスクの患者を見落とさないという観点から、最も高い値(平均値+標準誤差)を基準としてリスク分類を行っている。実際には標準誤差の範囲での変動も考慮しておくべきである。
中皮細胞面積は剥離細胞の計測であるため、まれに、何からの理由で剥離状態が変化し面積が大きく変化することがある(特に腹膜炎や腹部への強い物理的刺激など)。そのため、面積からの判断はOne Pointではなく連続した測定結果で判断することが望ましい。
リスク分類について
アルゴリズムは、PD中止基準と腹腔洗浄導入基準・中止基準に分けられる。PD中止基準はPD期間、中皮面積がリスクファクター、腹腔洗浄中止基準はPD中止時面積と洗浄時面積がリスクファクターである。PD中止基準としてLow risk、Middle risk、High riskの3群に、洗浄中止基準もLow risk、Middle risk、High riskの3群に分類される(図1)。
PD中止基準
Low risk 群(PD施行中面積<350 μ㎡ とPD期間<78ヶ月を満たす場合)
PD中止後のEPS発症率は0.1%。最も問題のない病期であり、PDの継続は可能である。PD中止後、抜管も可能である。PD中止または休息により腹膜組織の回復も見込まれ、PETの程度により中止後のPD再開も可能である。
Middle risk群(PD施行中面積≧350 μ㎡とPD期間≧78ヶ月のどちらかを満たす場合)
PD中止後のEPS発症率は8.3%。PD継続も可能であるが要観察の時期である。HD併用療法などの腹膜休息や中止後の洗浄も考慮すべきである。
High risk 群(PD施行中面積≧350 μ㎡とPD期間≧78ヶ月を満たす場合)
PD中止後のEPS発症率は42.9%。要観察の病期であり、PDの中止やHD併用療法などの腹膜休息も考慮すべきである。また、PDの継続は中止後の腹腔洗浄を前提に行うことが望ましい。
洗浄中止基準
Low risk 群(PD中止時面積<350 μ㎡と洗浄時面積<320 μ㎡を満たす場合)
洗浄中のEPS発症率は0.1%、洗浄中止後のEPS発症率は1.1%である。これ以上の洗浄継続の必要はなく抜管が可能である。
Middle risk群(PD中止時面積≧350 μ㎡と洗浄時面積≧320 μ㎡のどちらかを満たす場合)
洗浄中のEPS発症率は1.7%、洗浄中止後のEPS発症率は3.4%である。洗浄継続中止は可能であるが要観察である。
High risk群(PD中止時面積≧350 μ㎡と洗浄時面積≧320 μ㎡を満たす場合)
洗浄中のEPS発症率は29.6%、洗浄中止後のEPS発症率は不明であるが30%以上と推測される。また、洗浄時の面積は18~21か月以後は上昇傾向にあるため、18~21か月以内に洗浄時面積が320 μ㎡未満にならない場合は洗浄のみではEPSの予防は不可能であり、ステロイド等の単独/併用も考慮すべきである。しかし、この治療法に関する詳細なデータとエビデンスはない。
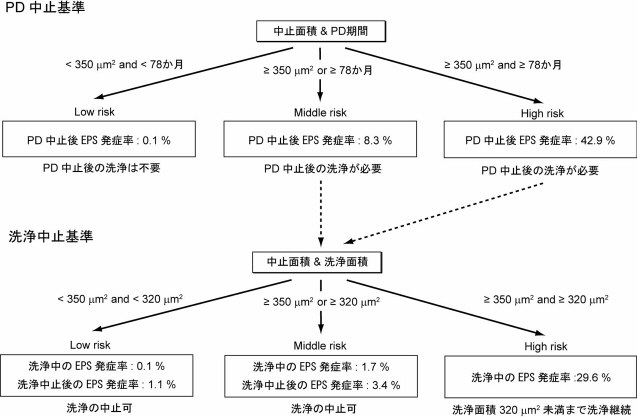
図1.PD中止および洗浄中止基準
アルゴリズムの注意点
- 1.洗浄中止基準でPD中止時面積が測定されていない場合には、これら基準を適用することができない。この場合のオプションとして、PD期間78か月を中止時面積に置き換えて、ある程度応用可能である。その時のEPS発症率はLow risk群(PD期間<78か月 and 洗浄時面積<320 μ㎡)で0.1%、Middle risk群(PD期間≧78か月 or 洗浄面積≧320 μ㎡)では3.5%、High risk群(PD期間≧78か月 and 洗浄面積≧320 μ㎡)では19.0%である(図2)。
- PD期間、中皮細胞面積では予測しえないEPSが存在する。中止基準としては他の臨床所見等ももちろん考慮されるべきである。また、PET値は有意な危険因子ではなかったため、アルゴリズムからは省いたが腹膜機能として重要な因子である。
- 今回のアルゴリズムは免疫抑制剤(ステロイド)を使用した症例は除いており、ステロイド使用症例では適応できないことがある。
注意:以上のデータはEBMの観点から統計学的に求められたものであり、確定診断ではない。
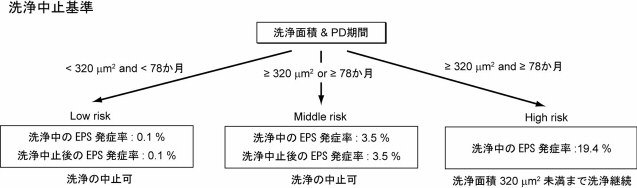
図2.中止時面積が不明の場合の洗浄中止基準
中皮細胞診の意義について
これまでの研究では、中皮細胞面積はPD期間と有意の相関を示すことが判明している。図3は、標準的なPD例(1.5%および2.5%使用)1460名での酸性透析液と中性透析液の中皮細胞面積の経時的変化を示したものである。中性液は酸性液に比べ面積は低いが、経年変化の傾きは同じである(73-96か月での低下はドロップアウトによる)。
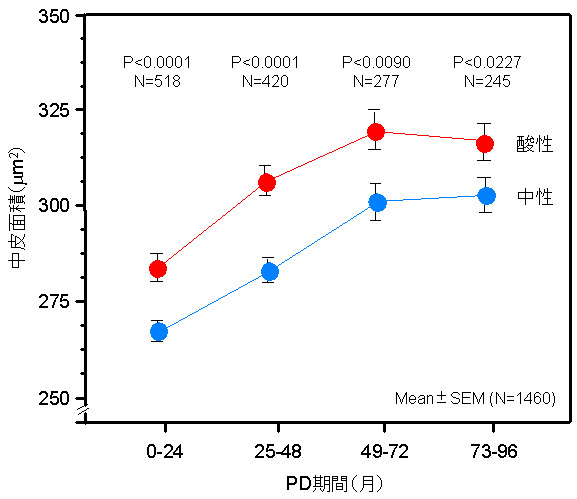
図3.PD症例での期間と面積(μ㎡)の関係
中皮細胞が腫大する理由として、(1)浸透圧などによる膨化、変形、(2)炎症などによる化生、(3)老化などによる腫大がある。PD排液での面積増大に関係しているのは、主に老化による腫大である。さらに、老化による腫大には、(Ⅰ)正常細胞分裂による減退(テロメア短縮をともなう)、(Ⅱ)老化様細胞増殖停止による減退(テロメア短縮をともなわない)の二つがある。実際には、PD液の非生体適合性因子によりこの二つの老化過程が中皮細胞に生じており、特に(Ⅱ)による傷害が、中皮細胞の腫大に大きく影響している。 老化による腫大はROS(reactive oxygen species)による酸化ストレスが最も大きな原因と考えられている。PD液におけるROSの主な発生源はグルコースとその分解物(GDPs)である(図4)。
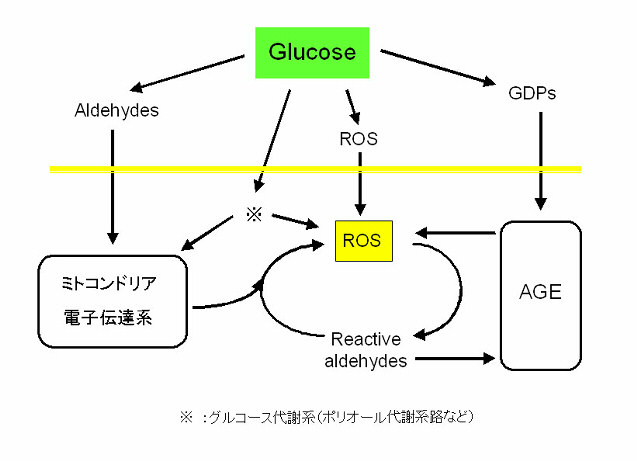
図4.グルコースとその分解物(GDPs)による酸化ストレス
すなわち、ROSによる傷害が大きいほど中皮細胞は腫大し、また正常老化における細胞life cycleも短縮されるため、中皮細胞の腫大(面積の増加)と中皮細胞の消失が生じる。排液中皮細胞診は、この中皮細胞の傷害の程度を排液中に遊離してくる中皮細胞の面積の平均値で示したものである。
以上の酸化ストレス原因の証明として、低GDPsである中性透析液の使用により、中皮細胞面積は低下し、また、PD+HD併用療法における週2日間の腹膜休息(PD液負荷の低減)においても面積は低下する(図5)。PD中止の場合19.8%、併用療法で12.8%、中性液で13.4%低下する。中皮細胞診は、腹膜における中皮細胞の傷害の程度だけを観察するものであるが、もし被嚢性腹膜硬化症(EPS)の発症機序が腹膜からの中皮細胞の脱落、それによる癒着、炎症が原因とするならば、中皮細胞診は一つの予防マーカーになると推測される。
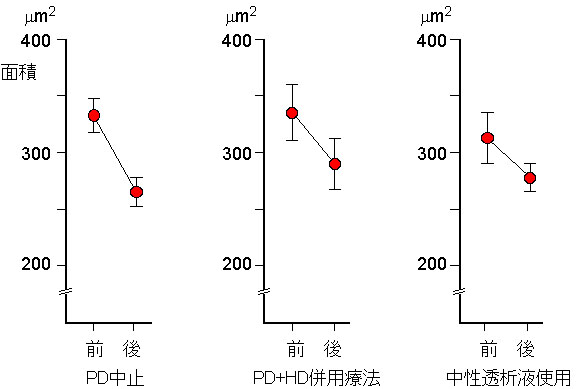
図5.各療法による中皮細胞面積の3か月後の変化。前の値はマッチングさせてある。
参考文献
- Yamamoto T, et al.: Morphological studies of mesothelial cells in CAPD effluent and their clinical significance. Am J Kidney Dis 1998;32;946-952
- Izumotani T, et al: Correlation between peritoneal mesothelial cell cytology and peritoneal histopathology with respect to prognosis in patients on continuous ambulatory peritoneal dialysis. Nephron 2001;89;43-49
- 山本忠司、他:排液中皮細胞診によるCAPD中止基準. 腹膜透析2002:334-337、2002
- 山本忠司、他:排液中皮細胞診による腹腔内洗浄の中止基準. 腹膜透析2002:338-341、2002
- 山本忠司、他:腹膜透析中止後腹膜洗浄中の被嚢性腹膜硬化症予防についてのコホート研究. 透析会誌2007;40;491-500
- 2009年版日本透析医学会「腹膜透析ガイドライン」. 透析会誌2009;42;285-315
- Yamamoto T, et al.: The role of peritoneal lavage and prognostic significance of mesothelial cell area in preventing encapsulating peritoneal sclerosis. Perit Dial Int 2010;30;343-352



